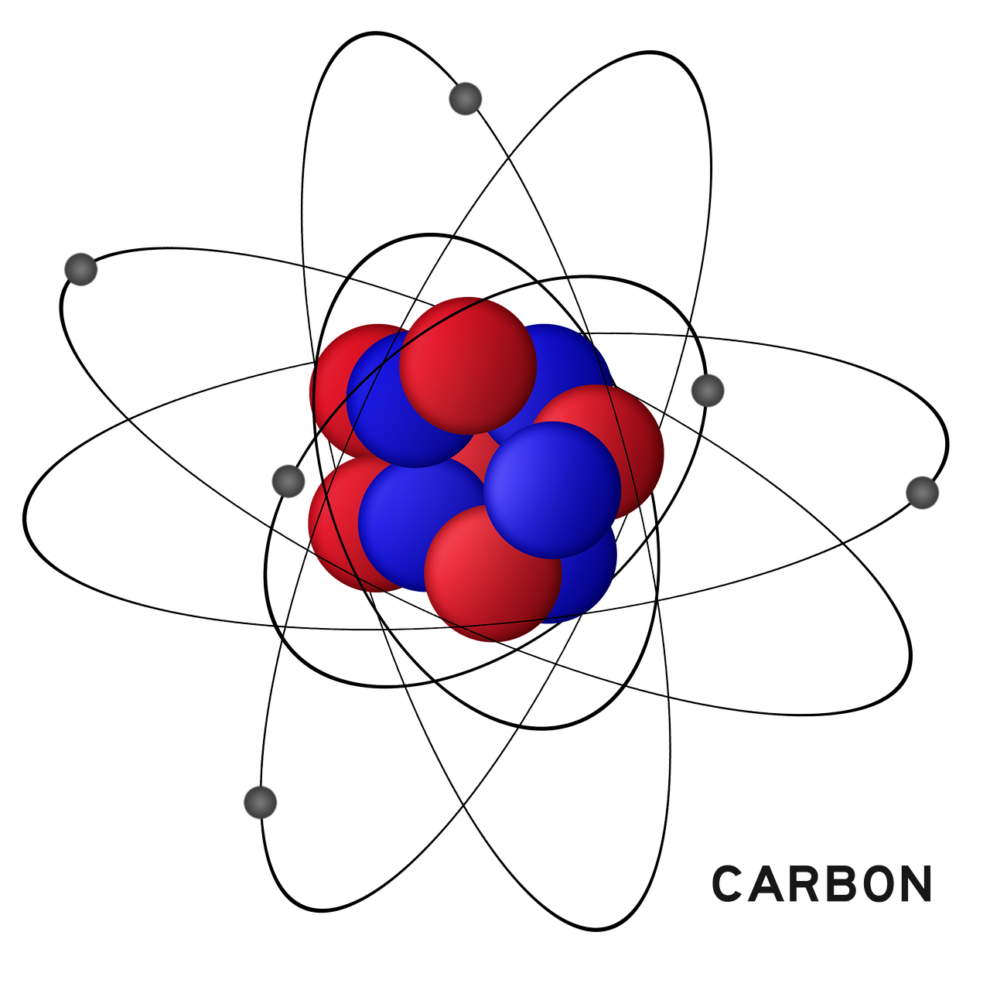
Lorsque nous sommes confrontés à des sujets tels que la chimie et la physique, il est impossible de ne pas affronter un sujet spécifique: la structure de l'atome. Comme nous le savons bien, l'atome est la plus petite particule d'un élément chimique et est à la base de toutes les substances organiques et inorganiques existantes.
Mais de quoi est l'atome lui-même?
Structure de l'atome
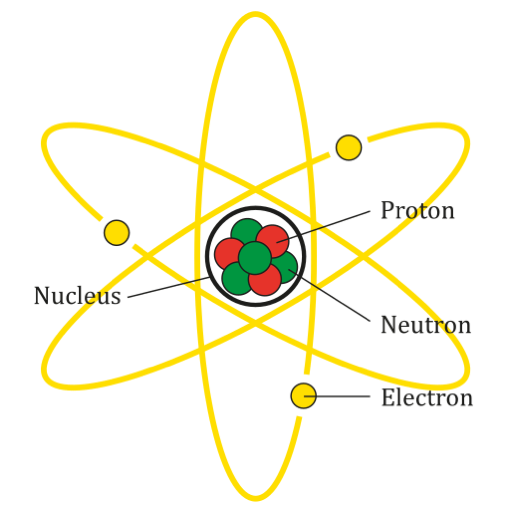
Tout d'abord, nous essayons de commencer par décrire une image générale: l'atome est composé d'un noyau, composé de protons et de neutrons, autour de laquelle les électrons orbit. Ces trois particules (protons, neutrons et électrons) prennent le nom de particules subatomiques et se démarquent les uns avec les autres pour la charge de masse et électrique.
Avant de continuer, il est important de définir ce dernier concept: ce que l'on entend par charge électrique.
La charge électrique est une propriété de la question qui est à la base de tous les phénomènes électriques et peut être de deux types: positif (signe +) et négatif (signe -).
Normalement, les corps ont une charge électrique neutre car elles contiennent une quantité égale de charges électriques positives et négatives qui s'annulent.
Cela dit, nous pouvons enfin aller pour analyser les particules subatomiques individuelles plus spécifiquement en commençant par l'électron.
Particules sous-atomiques
Électrons

Joseph John Thomson
Les électrons sont les plus petites particules avec une charge électrique négative et sont présents dans tous les atomes.
Ils ont été découverts en 1897 par le scientifique anglais Joseph John Thomson, à travers son expérience du tube Cathode Ray.
Ce que Thomson a fait, c'est de prendre un tube en verre, plein de gaz raréfiés, d'insérer deux électrodes à l'intérieur: l'anode (ayant une charge électrique positive) et la cathode (ayant une charge électrique négative). En réduisant la pression du gaz et en augmentant la charge électrique accumulée sur les électrodes, il a été possible de remarquer que la cathode était émise par les faisceaux lumineux, appelés rayons de cathode précisément.
Après avoir analysé ces faisceaux lumineux, il a été entendu qu'ils étaient formés par des particules de charge négatives, ayant une masse beaucoup plus faible que celle du plus petit atome existant (hydrogène). Après plus d'expériences, il a également été possible de remarquer que ces particules étaient toujours les mêmes, quel que soit le type de gaz qui se trouvait à l'intérieur du tube en verre.
Ces particules étaient précisément appelées électrons.
La charge électrique des électrons est également appelée charge élémentaire et applique de manière conventionnelle -1 C (Colomb). Cependant, selon le système international, la charge de l'électron (arrondi avec trois chiffres significatifs) est de -1 602 • 10-19 C.
Proton
La deuxième particule subatomique que nous allons examiner est le proton, ou la plus petite particule avec une charge électrique positive présente dans tous les atomes.

Ernest Ruthenford
Cela a été découvert vers le début du XXe siècle par le scientifique néo-zélandais Ernest Rutherford, qui a dirigé une expérience très similaire à celle du tube cathode de Thomson de Thomson: en prenant toujours un tube en verre, contenant le gaz raréfié, inséré correctement fier et une cathode d'anode à l'intérieur. Grâce à cette expérience, il a été possible de remarquer que derrière la cathode perforée, il a été créé une luminescence, obtenue à partir d'un mouvement de particules de l'anode, qui a constitué les rayons de canal So-appelés.
Ces particules étaient précisément les protons: elles avaient une charge électrique positive, une masse beaucoup plus grande que celle de l'électron et variaient selon le type de gaz contenu à l'intérieur du tube en verre.
La charge électrique du proton vaut de manière conventionnelle +1 C, alors qu'elle vaut +1 602 • 10-19 C, selon le système international.
Quant à sa masse, il s'agit de 1 007 U (unité de masse atomique).
Il est donc évident que malgré une masse beaucoup plus élevée que celle de l'électron (0,0005486 U), ces particules ont des charges électriques égales, mais du signe opposé. À cela s'ajoute le fait que dans un atome, nous trouvons toujours le même nombre de protons et d'électrons. Par conséquent, l'atome est électriquement neutre.
Neutron
Enfin, nous avons le neutron.
Les neutrons sont des particules de masse légèrement plus grandes que celles des protons et ont une charge électrique neutre. Ils ont été découverts en 1932 par le physicien anglais James Chadwick, à travers une expérience qui impliquait le α des particules de Polonio.
En entrant spécifiquement, Chadwick a observé que, bombardant un atome de béryllium avec le α des particules de Polonio, le Beerillium lui-même a pu produire un rayonnement pénétrant.
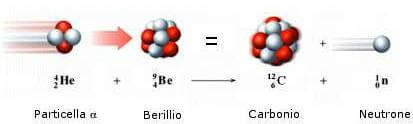
L'hypothèse de Chadwick était que ce rayonnement mystérieux était composé de toutes les mêmes particules. Ce dernier, comme ils ne ressentaient pas l'influence d'un champ électrique ou d'un champ magnétique, devaient nécessairement avoir une charge électrique neutre. Le terme neutrons est né précisément pour cette raison.
Les neutrons, contrairement aux protons et aux électrons, ne sont pas présents dans les atomes de tous les éléments: l'hydrogène est exception, dont les atomes sont complètement sans neutron.
Quant à leur masse, comme observé précédemment, les neutrons sont légèrement plus grands que les neutrons, avec une masse de 1,009 U.
De plus, exactement comme dans le cas des électrons, les caractéristiques des neutrons sont toujours les mêmes, quel que soit l'atome d'appartenance.
Nombre atomique et masse
Maintenant que nous avons analysé plus spécifiquement les particules subatomiques, nous pouvons passer aux deux derniers éléments fondamentaux à prendre en considération quand le prendre sur la structure de l'atome: le nombre atomique et le nombre de masse.
- Le nombre atomique (z) indique le nombre de protons présents dans le cœur de l'atome d'un élément et représente son identité chimique.
Le concept d'identité chimique est étroitement lié au modèle atomique de Dalton, selon lequel, dans les transformations chimiques, les noyaux des atomes impliqués restent inchangés. - Au lieu de cela, le nombre de masse (a) correspond au nombre total de neutrons et de protons présents à l'intérieur de l'atome d'un élément. Connaître le nombre de masse d'un atome est fondamental lorsque vous définissez la stabilité du noyau.
Avec cela, nous avons conclu notre analyse sur la structure de l'atome.